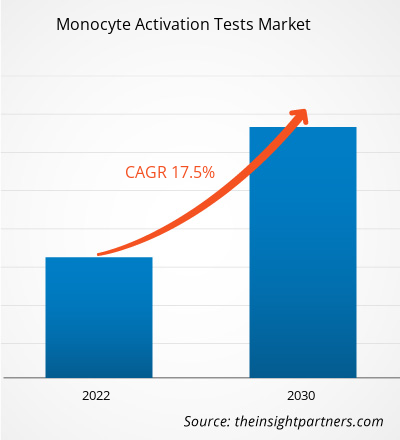
単球活性化検査市場規模は、2031年までに16億3,000万米ドルに達すると予想されています。市場は2025年から2031年の間に14.6%のCAGRを記録すると予想されています。
アナリストの視点
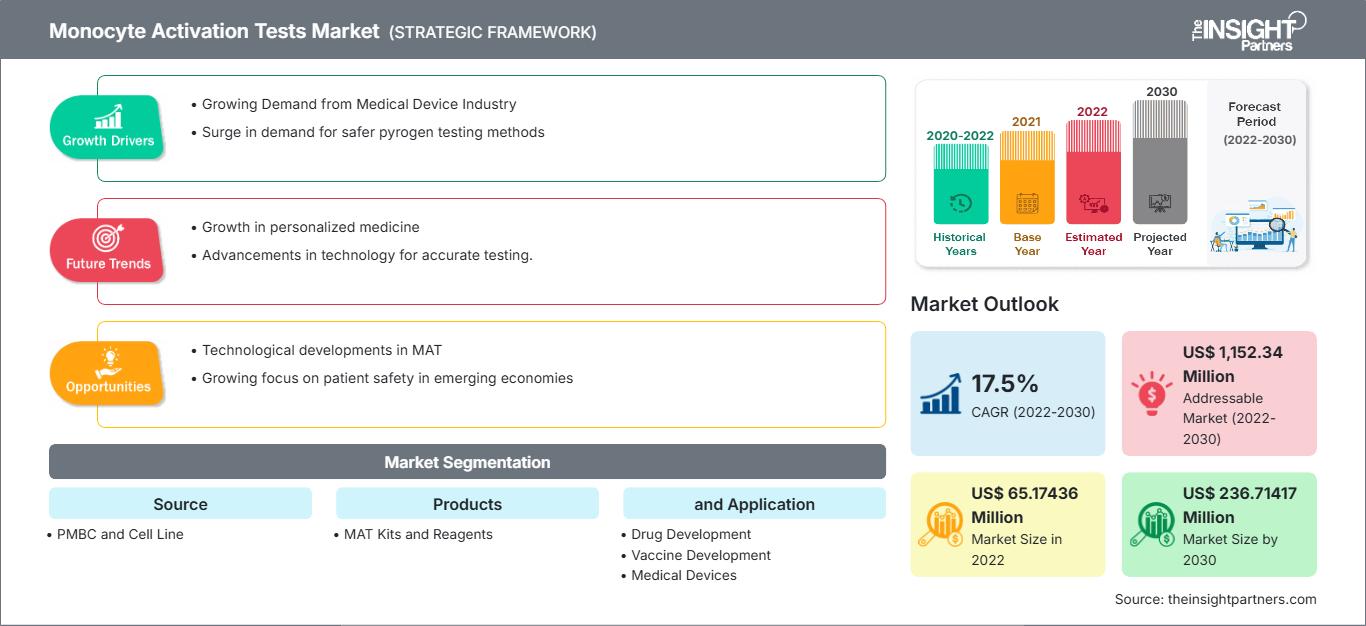
単球活性化試験市場分析には、患者の安全性への懸念の高まりや、製薬、バイオテクノロジー、医療機器などのエンドユーザー産業におけるより安全な発熱物質検査法の需要の急増といった市場牽引要因の分析が含まれています。さらに、単球活性化試験法の技術開発は、予測期間中に単球活性化試験市場の成長を促進すると予想されます。
情報源に基づいて、単球活性化試験市場はPMBCと細胞株に分かれています。PMBCセグメントは2022年に大きなシェアを占め、予測期間中も同様の傾向が続くと予想されます。製品に基づいて、単球活性化試験市場はMATキットと試薬に分かれています。MATキットセグメントは2022年に大きなシェアを占め、予測期間中も同様の傾向が続くと予想されます。一方、試薬セグメントは予測期間中に高いCAGRを記録すると予想されます。用途に基づいて、単球活性化試験市場は、医薬品開発、ワクチン開発、医療機器、その他(研究など)に分割されています。医薬品開発セグメントは2022年に最大のシェアを獲得し、2022年から2030年まで同じ傾向が見られると予想されます。
単球活性化試験は、エンドトキシンと非エンドトキシン発熱物質の相乗効果によって増強されたサイトカイン放出を検出します。単球活性化試験(MAT)は、非経口医薬品、生物製剤、および医療機器をあらゆる分類の発熱物質について試験するために設計されたin vitro試験です。過去5年間、放出試験としてウサギ発熱物質試験を使用していたワクチンは、単球活性化試験(MAT)を最初に採用したワクチンの一つです。さらに、MATとは異なり、細菌エンドトキシン試験は、本質的に発熱性である製品や、試験に影響を与える傾向がある水酸化アルミニウムなどのワクチンに一般的に含まれる添加物を含む製品には適さないことがよくあります。 MAT がワクチンの試験に取り入れた例としては、髄膜炎菌ワクチン、高免疫血清、髄膜炎菌ワクチン、黄熱病ワクチン、赤痢菌ワクチン、狂犬病ワクチン、B 型肝炎ワクチン、ダニ媒介性脳炎ウイルスワクチンなどがあります。
要件に合わせてレポートをカスタマイズ
無料カスタマイズ単球活性化検査市場:戦略的洞察
-
このレポートの主要な市場動向を入手してください。この無料サンプルには、市場動向から見積もりや予測に至るまでのデータ分析が含まれます。
市場洞察
医療機器業界からの需要増加
単球活性化試験(MAT)は、細菌、真菌、ウイルスなどの発熱物質を検出および定量化するヒト細胞ベースの試験です。MATは、処理した血液細胞からのサイトカイン放出を測定するためにELISAアッセイを使用します。MATは広く利用可能ですが、医療機器の生体適合性評価のための動物ベースの発熱物質試験の代わりに使用されることはほとんどありません。国立毒性プログラム代替毒性学的手法評価のための機関間センター(NICEATM)とPETA国際科学コンソーシアム(PISC)は、医療機器試験におけるMATの使用実装に必要な手順を詳しく説明することを目的として、2018年9月に国立衛生研究所でワークショップを開催しました。DXCテクノロジーグループのLuxoftによると、医療機器は、予測アルゴリズムと患者データ分析を通じて正確な診断、効果的な治療、個別化されたケアを提供することで、ヘルスケアのデジタル変革を支援しています。個別化医療、インプラント機器、スマート医療機器、非侵襲手術における技術進歩は、より良いケア、患者アウトカムの改善、そしてコスト削減を実現することで、ヘルスケア業界全体に革命をもたらしています。医療機器業界の成長は、現在、単球活性化試験法の成長を促しており、予測期間中も同様の傾向が続くと予想されます。
市場機会
単球活性化試験法の技術開発
単球活性化試験法は、主に動物実験の代替法として導入され、ヒトin vitro系における発熱物質試験の実施機会を提供することを目的としていました。単球活性化試験(MAT)は、国際的な検証の公表を受け、2010年に欧州薬局方(EP)に導入されました。市場参加者によるMATアッセイおよび試薬の継続的な革新と開発により、再現性、感度、特異性が大幅に向上し、発熱物質検出における信頼性と安全性が向上しました。MATアッセイは、医薬品や医療機器などの非経口製品中のエンドトキシンおよび非エンドトキシン発熱物質の検出に用いられます。通常、MATは規制ガイドラインに準拠した従来の動物実験に代わるin vitro代替法となります。ウサギ発熱物質試験とリムルスアメーボサイトライセート(LAL)試験は、発熱物質検出に広く用いられています。どちらの方法も動物を用い、いくつかの限界があります。ウサギ発熱物質試験は、動物の反応がヒトの反応と異なる可能性があるため、堅牢性に欠けるという問題があります。さらに、LAL試験ではエンドトキシンのみが検出されるため、検査対象サンプル中に存在する可能性のあるエンドトキシン以外の発熱物質が無視され、安全性リスクが生じます。そのため、これらの限界を克服するため、2010年に欧州薬局方においてウサギ発熱物質試験(EP Chapter 2.6.30)に代わる公定法として単球活性化試験(MAT)が規定され、FDAの業界向けガイダンスにも明記されました。市場参加者によるMATアッセイおよび試薬の継続的な革新と開発により、再現性、感度、特異性が大幅に向上し、MATは発熱物質検出における信頼性と安全性を高める選択肢となっています。
レポートのセグメント化と範囲
ソースベースの洞察
ソースに基づいて、単球活性化テスト市場は、PMBCと細胞株に分かれています。PMBCセグメントは2022年に大きなシェアを占め、予測期間中に同様の傾向が続くと予想されます。同じセグメントは、2022年から2030年にかけてより高いCAGRを示すことが予想されます。現在、世界中で入手可能な市販の単球活性化テスト用細胞ソースは、Mono-Mac-6(MM6)細胞株と末梢血単核細胞(PBMC)の2つです。MM6は、1人の急性単球性白血病患者の血液に由来するため、単球は、発熱性汚染物質を一貫して検出し、健康なヒトによるサイトカインの放出を開始するために必要な安定した発現を反映するTLRを持たない場合があります。したがって、この細胞ソースを使用したMAT結果の再現性は低いことがわかりました。 (2.6.30)では、MM6ベースのMATキットは、非エンドトキシン性発熱物質の検出能力が「限定的」であるとも述べられています。一方、PBMCベースのMATキットは、スクリーニングを受けた健康なドナーのプール血液からPBMCを採取します。つまり、添加された製品サンプルとインキュベートすると、単球活性化プロセスによって健康なヒトの成長が促進される可能性があります。その結果、この細胞源に基づくMATキットの結果は一貫して再現性があることが確認されています。Ph. Eur. (2.6.30)では、この細胞源はエンドトキシンと非エンドトキシン性発熱物質の両方の検出に優れているとされています。
現在、市場にはPBMCベースの単球活性化試験を市販しているベンダーが3社あります。それぞれのLoDは0.125 EU/ml、0.02 EU/ml、0.016 EU/mlです。CTL-MATアッセイは、市場をリードするLoD 0.004 EU/mlを誇り、世界で最も感度の高い単球活性化試験となっています。
製品ベースのインサイト
製品別に見ると、単球活性化検査市場はMATキットと試薬に分かれています。MATキットセグメントは2022年に大きなシェアを占め、予測期間中も同様の傾向が続くと予想されます。一方、試薬セグメントは予測期間中に高いCAGRを記録すると予想されます。
アプリケーションベースの洞察
アプリケーションに基づいて、単球活性化テスト市場は、医薬品開発、ワクチン開発、医療機器、その他(研究など)に分類されています。医薬品開発セグメントは2022年に最大のシェアを獲得し、2022年から2030年まで同じ傾向が見込まれています。国立医学図書館によると、医薬品は患者の生活の質の向上に貢献してきた新興有機化合物のグループです。製薬部門は、ブランド医薬品とジェネリック医薬品の製造、開発、販売に携わっています。2014年に初めて、世界中の医薬品の総収益が1兆米ドルを超えました。医薬品市場は2017年以降、年率5.8%で拡大しています。同年、世界の医薬品市場の収益は1兆1,430億米ドルで、2021年には1兆4,620億米ドルに達しました。単球活性化テスト(MAT)は、非経口薬、生物製剤、医療機器をすべての分類の発熱物質についてテストするように設計されています。非経口投与される医薬品は、発熱性物質(発熱物質)による汚染があってはなりません。これらの物質は、患者の自然免疫系に生命を脅かす全身反応を引き起こす可能性があるためです。これは、患者に投与する前に、生物学的製剤に発熱物質が混入していないことを確認するためです。当初、RPTと細菌エンドトキシン試験(BET)/リムルスアメーバ細胞溶解物試験(LAL)は、ex vivo試験の選択肢として使用されてきました。しかし、動物実験法に関する厳格な規制により、市場参加者は、このような動物実験法の使用を最小限に抑える代替方法の開発を余儀なくされました。RPTとBETの限界、そして複雑な製品の製造増加を考慮し、欧州薬局方は、人道的な免疫反応をシミュレートし、RPTの利点(グラム陰性エンドトキシンを超える発熱性の評価)とin vitro試験の利点を組み合わせたMAT活性化試験法を導入しました。 RPTとは対照的に、MATは動物を使用せずに完全に定量的な試験として適用できるため、本質的に発熱性があり、ヒト細胞を使用するため生理学的に重要なワクチンに適しています。MAT試験アッセイは、血液由来製品、細胞由来製品、生物製剤、ワクチンを検出できます。また、MAT試験法は、幅広い医薬品や医療機器、さらにはin vivo試験が不可能な製品(例えば、ヒアルロン酸を含む製品)も検出できます。こうした要因は近年、単球活性化試験市場全体を後押ししており、予測期間中も同様の傾向が続くと予想されます。
単球活性化試験市場の地域別分析
予測期間全体を通して単球活性化検査市場に影響を与える地域的な傾向と要因は、The Insight Partnersのアナリストによって徹底的に説明されています。このセクションでは、北米、ヨーロッパ、アジア太平洋、中東・アフリカ、中南米における単球活性化検査市場のセグメントと地域についても説明します。
単球活性化試験市場レポートの範囲
| レポート属性 | 詳細 |
|---|---|
| 2024年の市場規模 | XX百万米ドル |
| 2031年までの市場規模 | 16億2,980万米ドル |
| 世界のCAGR(2025年~2031年) | 14.6% |
| 履歴データ | 2021-2023 |
| 予測期間 | 2025~2031年 |
| 対象セグメント |
出典別
|
| 対象地域と国 |
北米
|
| 市場リーダーと主要企業の概要 |
|
単球活性化試験市場のプレーヤー密度:ビジネスダイナミクスへの影響を理解する
単球活性化試験市場は、消費者の嗜好の変化、技術の進歩、製品の利点に対する認知度の高まりといった要因によるエンドユーザーの需要増加に牽引され、急速に成長しています。需要の増加に伴い、企業は製品ラインナップの拡充、消費者ニーズへの対応のための革新、そして新たなトレンドの活用を進めており、これが市場の成長をさらに加速させています。
- 単球活性化テスト市場のトップキープレーヤーの概要を入手
地域分析
地域別に見ると、単球活性化検査市場は北米、欧州、アジア太平洋、中南米、中東・アフリカに分類されます。北米は2022年に最大の市場シェアを獲得し、予測期間中も同様の傾向を維持すると予想されており、欧州がそれに続きます。米国薬局方(USP)やカナダ政府などの機関による単球活性化検査の規制は、この地域における単球活性化検査市場全体の成長をさらに促進しています。また、患者の安全性への懸念と医療成果の向上への関心の高まりも、北米における市場成長を後押しする要因の一つとなっています。
単球活性化試験市場で事業を展開している大手企業としては、ドイツ・ダルムシュタットの Merck KGaA およびその関連会社、Charles River Laboratories International, Inc.、Thermo Fisher Scientific、Sanquin、Lonza Group などがあります。
ロンザは2023年10月、ウサギを使わない発熱物質試験の効率化と簡便化を実現する2つの新しい迅速単球活性化試験(MAT)システム、「PyroCell MAT Rapid System」と「PyroCell MAT Human Serum (HS) Rapid System」を発売しました。これらのシステムは、ロンザの従来のMATシステムキットに代わるもので、新たに発売された製品には、作業時間を最小限に抑え、結果が出るまでの時間を2日から2時間に短縮する新しいPeliKine Human IL-6 Rapid ELISA Kitが含まれています。これらの新しい検査により、製薬会社やバイオテクノロジー会社は、製品安全性試験においてMAT試験をより容易に実施できるようになり、動物実験への依存度を低減できます。
- 過去2年間の分析、基準年、CAGRによる予測(7年間)
- PEST分析とSWOT分析
- 市場規模価値/数量 - 世界、地域、国
- 業界と競争環境
- Excel データセット
最新レポート
お客様の声
購入理由
- 情報に基づいた意思決定
- 市場動向の理解
- 競合分析
- 顧客インサイト
- 市場予測
- リスク軽減
- 戦略計画
- 投資の正当性
- 新興市場の特定
- マーケティング戦略の強化
- 業務効率の向上
- 規制動向への対応





















 無料サンプルを入手 - 単球活性化試験市場
無料サンプルを入手 - 単球活性化試験市場