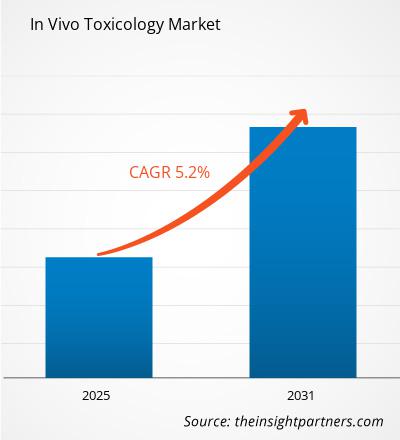
Le marché de la toxicologie in vivo devrait atteindre 8,19 milliards de dollars américains d'ici 2031. Il devrait enregistrer un TCAC de 8,5 % entre 2025 et 2031.
L'étude de marché sur la toxicologie in vivo segmente le marché par type de produit : instruments, réactifs et logiciels. Les applications analysées comprennent la toxicité systémique, la toxicité spécifique à un organe et d'autres. Les utilisateurs finaux couverts par l'étude sont les entreprises pharmaceutiques, les établissements d'enseignement et de recherche, ainsi que les organismes de recherche sous contrat (CRO). L'analyse régionale couvre l'Amérique du Nord, l'Europe, l'Asie-Pacifique, le Moyen-Orient et l'Afrique, et l'Amérique du Sud. L'évaluation du marché est exprimée en dollars américains pour toutes les analyses segmentaires.
Objectif du rapport
Le rapport sur le marché de la toxicologie in vivo, réalisé par The Insight Partners, vise à décrire le paysage actuel et la croissance future, les principaux facteurs de croissance, les défis et les opportunités. Cela permettra d'éclairer divers acteurs économiques, tels que :
- Fournisseurs de technologies/Fabricants : Pour comprendre l'évolution de la dynamique du marché et identifier les opportunités de croissance potentielles, afin de prendre des décisions stratégiques éclairées.
- Investisseurs : Pour réaliser une analyse approfondie des tendances concernant le taux de croissance du marché, les projections financières et les opportunités tout au long de la chaîne de valeur.
- Organismes de réglementation : Pour encadrer les politiques et les activités du marché afin de minimiser les abus, préserver la confiance des investisseurs et garantir l'intégrité et la stabilité du marché.
Segmentation du marché de la toxicologie in vivo : Produits
- Instruments
- Modèles animaux
- Réactifs et kits
Type de test
- Tests de toxicité chronique
- Tests de toxicité subchronique
- Tests de toxicité subaiguë
- Tests de toxicité aiguë
Critères d’évaluation de la toxicité
- Immunotoxicité
- Toxicité systémique
- Cancérogénicité
- Génotoxicité
- Toxicité pour le développement et la reproduction
Vous bénéficierez d’une personnalisation sur n’importe quel rapport - gratuitement - y compris des parties de ce rapport, ou une analyse au niveau du pays, un pack de données Excel, ainsi que de profiter d’offres exceptionnelles et de réductions pour les start-ups et les universités
Marché de la toxicologie in vivo: Perspectives stratégiques
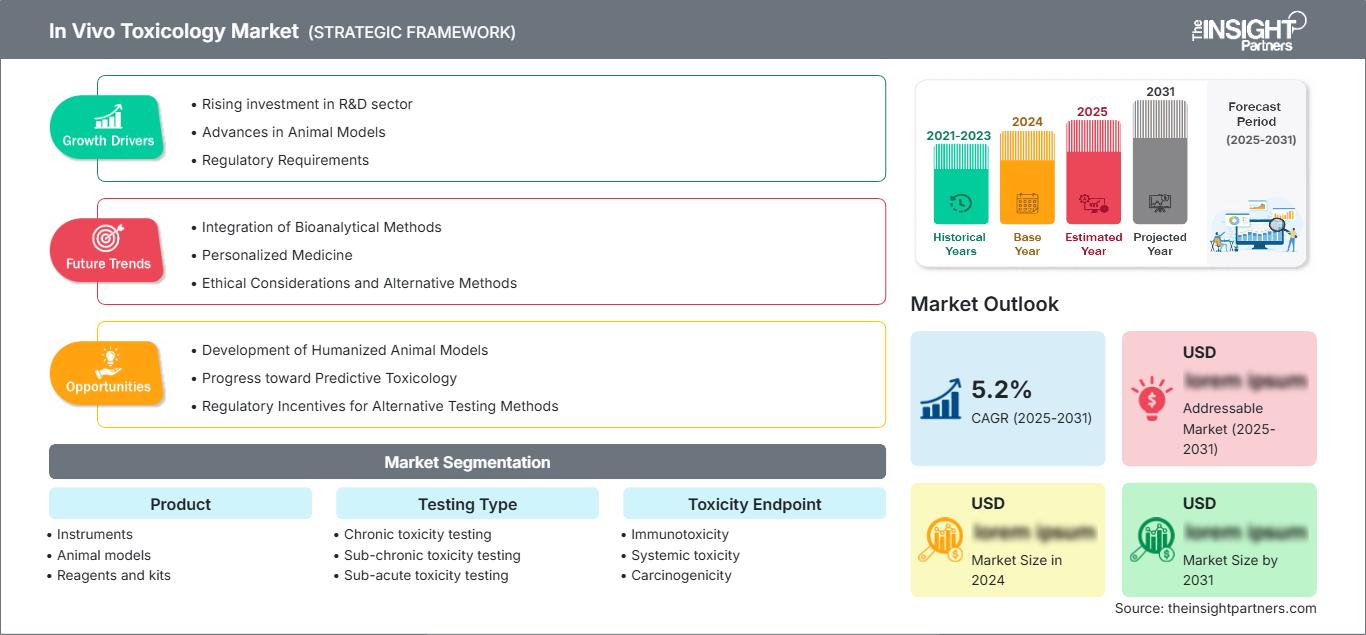
-
Obtenez les principales tendances clés du marché de ce rapport.Cet échantillon GRATUIT comprendra une analyse de données, allant des tendances du marché aux estimations et prévisions.
Facteurs de croissance du marché de la toxicologie in vivo
- Investissements croissants dans la R&D : Les investissements importants dans la R&D pharmaceutique sont étroitement liés à la demande en toxicologie in vivo. Face à la découverte et au développement constants de nouvelles entités chimiques (NCE), les entreprises pharmaceutiques exigent des données de sécurité fiables et complètes pour chaque NCE avant de passer aux essais cliniques chez l’humain. Selon l’OMS, environ 10 000 NCE sont testées chaque année, mais seulement 250 d’entre elles environ font l’objet d’essais cliniques. Par conséquent, des tests de sécurité efficaces sont primordiaux. La toxicologie in vivo jouera un rôle essentiel en identifiant les risques de toxicité potentiels le plus tôt possible au cours du développement, évitant ainsi des échecs coûteux lors des essais cliniques de phase avancée. Les chercheurs pourront observer les effets physiologiques et les réponses des nouveaux composés en développement chez les organismes vivants, garantissant ainsi que seuls les produits les plus sûrs progressent dans la chaîne de développement, un aspect essentiel tant pour la sécurité des patients que pour l'approbation réglementaire. Progrès des modèles animaux : Les progrès réalisés dans le domaine des modèles animaux, notamment les OGM et les modèles spécifiques à certaines maladies, ont considérablement accru la validité des études de toxicologie in vivo. Ces modèles avancés représentent mieux la biologie humaine, comblant ainsi le fossé entre les résultats précliniques et cliniques. Par exemple, les souris génétiquement modifiées, comme la souris Knockout, sont conçues pour être dépourvues de certains gènes. Cela permet aux chercheurs d'étudier l'effet de la suppression de certains composants génétiques sur la toxicité des substances. En effet, les OGM sont de plus en plus utilisés pour modéliser des maladies humaines, telles que le cancer ou la maladie d'Alzheimer, et pour tester les réponses potentielles aux médicaments, améliorant ainsi la prédictibilité des études in vivo. Ces progrès ont été soutenus par des investissements substantiels dans les biotechnologies, les dépenses mondiales consacrées aux organismes génétiquement modifiés devant dépasser 10 milliards de dollars d'ici 2026, renforçant ainsi les capacités de la recherche en toxicologie. Exigences réglementaires : Différentes régions imposent des exigences réglementaires strictes, telles que la Food and Drug Administration (FDA) aux États-Unis et l'Agence européenne des médicaments (EMA), qui exigent que les médicaments et les produits chimiques soient validés par des études de toxicologie in vivo avant leur mise sur le marché. Par exemple, la FDA exige que les nouveaux médicaments subissent des tests précliniques, comme des études in vivo, afin de déterminer leur toxicité sur les organes et les tissus. Le plus souvent, ces tests sont déterminants pour l'autorisation de mise sur le marché ou le passage aux essais cliniques. L'importance du strict respect de ces procédures réglementaires est capitale, car les produits non conformes aux normes de sécurité sont systématiquement rejetés ou font l'objet de retards importants. Ainsi, les tests de toxicologie in vivo demeurent une composante essentielle du processus d'approbation réglementaire d'un produit, garantissant sa sécurité pour les consommateurs.
Tendances futures du marché de la toxicologie in vivo
- Intégration des méthodes bioanalytiques : L'intégration des techniques bioanalytiques en toxicologie in vivo a transformé l'étude des effets toxiques. Des techniques telles que la spectrométrie de masse, la chromatographie et la bio-imagerie sont de plus en plus utilisées pour suivre et quantifier les substances dans l'organisme. Par exemple, la spectrométrie de masse permet de mesurer la concentration des médicaments et de leurs métabolites dans les tissus biologiques, offrant ainsi une image plus précise de leurs effets nocifs potentiels. Ces progrès ont permis aux chercheurs de détecter la toxicité à des doses encore plus faibles, contribuant à améliorer la précision et la rapidité des évaluations de sécurité. L'application des techniques bioanalytiques joue également un rôle clé dans le suivi de l'exposition à long terme aux substances par les principaux organes, une tâche impossible avec les seules méthodes traditionnelles. L'adoption accrue de ces techniques dans les tests toxicologiques garantit que les médicaments et les produits chimiques sont sûrs non seulement pour une utilisation à court terme, mais aussi pour une exposition prolongée, ce qui représente une préoccupation croissante dans le traitement des maladies chroniques et la protection de l'environnement. Médecine personnalisée : Avec l'essor de la médecine personnalisée, les études toxicologiques in vivo évoluent pour tenir compte de la variabilité génétique interindividuelle. La médecine personnalisée vise à adapter les traitements au profil génétique spécifique de chaque patient, afin d'en améliorer l'efficacité et de réduire les effets indésirables. Ce changement de paradigme implique notamment l'application du profilage génétique aux tests toxicologiques in vivo, permettant de prédire comment un médicament pourrait interagir avec des variants génétiques spécifiques chez un patient donné. En oncologie, des thérapies ciblées ont été conçues pour interagir avec les mutations spécifiques présentes dans les cellules cancéreuses. Des études ont démontré que jusqu'à 30 % des patients atteints de cancer souffrent d'effets indésirables liés aux médicaments en raison de variations génétiques des enzymes métabolisant les médicaments. La toxicologie in vivo peut désormais être intégrée aux approches personnalisées, permettant ainsi de mieux prédire les réponses individuelles aux médicaments et, à terme, de réduire le risque d'effets secondaires nocifs tout en améliorant les résultats des traitements. Considérations éthiques et méthodes alternatives : Les préoccupations éthiques liées à l'expérimentation animale ont suscité un intérêt pour les méthodes d'essai alternatives, une tendance majeure en toxicologie in vivo. Bien que les modèles animaux restent les plus utilisés, on observe une volonté croissante de réduire leur recours en raison de préoccupations éthiques relatives au bien-être animal. D'autres méthodes d'essai alternatives, telles que les essais in vitro et la technologie des organes sur puce, qui peuvent reproduire les conditions in vivo sans utiliser d'animaux, sont en cours de développement. Le règlement de l'Union européenne, REACH (enregistrement, évaluation, autorisation et restriction des substances chimiques), a fixé des objectifs précis pour l'expérimentation animale, et les entreprises se tournent de plus en plus vers des alternatives innovantes. Malgré cela, les études in vivo restent indispensables pour certains critères d'évaluation de la toxicité, tels que les études de cancérogénicité à long terme, qui ne peuvent être reproduits par des méthodes in vitro. Par conséquent, on observe une tendance vers une approche hybride où les tests in vivo sont complétés par des modèles in vitro et informatiques afin de réduire l'utilisation d'animaux sans compromettre la rigueur scientifique.
Opportunités du marché de la toxicologie in vivo
- Développement de modèles animaux humanisés : Les modèles animaux humanisés sont très prometteurs pour le marché de la toxicologie in vivo. Ils sont génétiquement modifiés pour exprimer des gènes, des tissus ou des systèmes immunitaires humains, imitant ainsi plus fidèlement la biologie humaine. Les données obtenues grâce à ces modèles humanisés permettraient de mieux prédire les réponses humaines, notamment en matière de métabolisme des médicaments, de réponse immunitaire et de progression de la maladie. Par exemple, des modèles de souris humanisées sont utilisés pour étudier les résultats de nouvelles approches thérapeutiques anticancéreuses, offrant une plateforme plus fiable pour tester l'efficacité et l'innocuité des médicaments. La tendance mondiale vers des méthodes de test plus personnalisées et adaptées à l'humain devrait favoriser l'adoption de modèles humanisés en toxicologie, offrant ainsi aux entreprises l'opportunité d'innover dans ce domaine et de répondre à la demande croissante de méthodes de test de sécurité plus prédictives, plus humaines et plus précises. Progrès vers la toxicologie prédictive : Avec le temps, les études in vivo intègrent la toxicologie prédictive, ce qui accélère la découverte de médicaments en ce qui concerne leur sécurité et leur efficacité. Désormais, les entreprises qui intègrent des simulations informatiques à l'intelligence artificielle et à l'apprentissage automatique dans les études toxicologiques permettent de détecter les effets toxiques beaucoup plus tôt dans le processus de développement des médicaments. La recherche utilise des technologies de pointe, telles que l'analyse de données massives issues d'expériences in vivo. Ces technologies utilisent des algorithmes pour prédire l'effet des composés médicamenteux sur différents organes ou tissus. Des modèles d'IA, par exemple, sont développés pour prédire la cardiotoxicité des nouveaux médicaments afin de réduire le nombre d'essais sur les animaux, longs et coûteux. À mesure que la capacité à prédire la toxicité avec plus de précision s'améliore, le recours aux modèles prédictifs en toxicologie augmentera, réduisant potentiellement le besoin global d'études in vivo traditionnelles. Ceci représente une formidable opportunité d'innovation, les entreprises développant et perfectionnant des outils prédictifs pour améliorer la sécurité des médicaments et rationaliser le processus de développement pharmaceutique. Incitations réglementaires aux méthodes d'essai alternatives : Les organismes de réglementation encouragent de plus en plus le développement de méthodes d'essai alternatives permettant d'éviter ou de remplacer l'expérimentation animale. Par exemple, la loi américaine « 21st Century Cures Act » de la FDA encourage le développement de technologies innovantes, notamment de méthodes d'essai alternatives, pour évaluer la sécurité des médicaments et des produits chimiques. Les agences soutiennent l'utilisation de modèles in silico, de cultures tissulaires 3D et de plateformes d'organes sur puce dans le cadre réglementaire. Cette approche ne se limite pas aux considérations éthiques, mais prend également en compte l'accélération du rythme des essais et les économies réalisées par rapport aux essais sur les animaux. Les entreprises qui peuvent tirer profit de ces changements réglementaires sont notamment celles qui peuvent investir dans des méthodes alternatives pour obtenir des procédures d'autorisation de mise sur le marché plus rapides et répondre à la pression croissante du public et des institutions en faveur de la réduction des tests sur les animaux.
Marché de la toxicologie in vivo
Les analystes de The Insight Partners ont analysé en détail les tendances régionales et les facteurs influençant le marché de la toxicologie in vivo tout au long de la période prévisionnelle. Cette section aborde également les segments et la répartition géographique du marché de la gestion des troubles du rythme cardiaque en Amérique du Nord, en Europe, en Asie-Pacifique, au Moyen-Orient et en Afrique, ainsi qu'en Amérique du Sud et centrale.
Portée du rapport sur le marché de la toxicologie in vivo
| Attribut de rapport | Détails |
|---|---|
| Taille du marché en 2024 | US$ 4.63 Billion |
| Taille du marché par 2031 | US$ 8.19 Billion |
| TCAC mondial (2025 - 2031) | 8.5% |
| Données historiques | 2021-2023 |
| Période de prévision | 2025-2031 |
| Segments couverts |
By Produits
|
| Régions et pays couverts |
Amérique du Nord
|
| Leaders du marché et profils d'entreprises clés |
|
Densité des acteurs du marché de la toxicologie in vivo : comprendre son impact sur la dynamique commerciale
Le marché de la toxicologie in vivo connaît une croissance rapide, portée par une demande croissante des utilisateurs finaux, elle-même alimentée par l'évolution des préférences des consommateurs, les progrès technologiques et une meilleure connaissance des avantages du produit. Face à cette demande grandissante, les entreprises élargissent leur offre, innovent pour répondre aux besoins des consommateurs et tirent parti des tendances émergentes, ce qui stimule davantage la croissance du marché.
- Obtenez le Marché de la toxicologie in vivo Aperçu des principaux acteurs clés
Points clés de vente
- Couverture exhaustive : Ce rapport analyse en détail les produits, services, types et utilisateurs finaux du marché de la toxicologie in vivo, offrant ainsi une vision globale.
- Analyse d'experts : Ce rapport repose sur une connaissance approfondie du secteur et des analystes.
- Informations actualisées : Grâce à sa couverture des informations et tendances les plus récentes, ce rapport garantit la pertinence de vos analyses.
- Options de personnalisation : Ce rapport peut être personnalisé pour répondre aux besoins spécifiques de chaque client et s'adapter parfaitement à ses stratégies commerciales.
Ce rapport d'étude de marché sur la toxicologie in vivo peut donc vous aider à décrypter et comprendre le contexte sectoriel et les perspectives de croissance. Malgré quelques points à améliorer, les avantages de ce rapport l'emportent généralement sur les inconvénients.
- Analyse historique (2 ans), année de base, prévision (7 ans) avec TCAC
- Analyse PEST et SWOT
- Taille du marché Valeur / Volume - Mondial, Régional, Pays
- Industrie et paysage concurrentiel
- Ensemble de données Excel
Témoignages
Raison d'acheter
- Prise de décision éclairée
- Compréhension de la dynamique du marché
- Analyse concurrentielle
- Connaissances clients
- Prévisions de marché
- Atténuation des risques
- Planification stratégique
- Justification des investissements
- Identification des marchés émergents
- Amélioration des stratégies marketing
- Amélioration de l'efficacité opérationnelle
- Alignement sur les tendances réglementaires














Débloquez des remises exclusives sur les rapports
Demander maintenant









 Obtenez un échantillon gratuit pour - Marché de la toxicologie in vivo
Obtenez un échantillon gratuit pour - Marché de la toxicologie in vivo