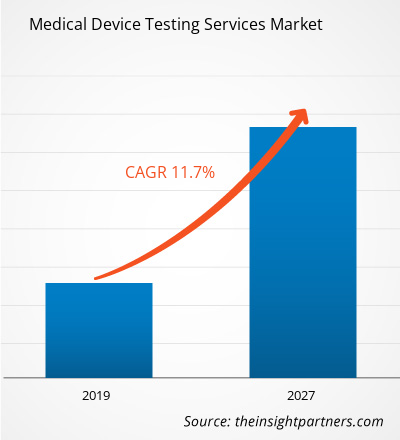
El mercado de servicios de pruebas de dispositivos médicos en el sector sanitario se valoró en 5.505,4 millones de dólares estadounidenses en 2018 y se prevé que alcance los 14.660,1 millones de dólares estadounidenses en 2027; se espera que crezca a una tasa de crecimiento anual compuesta (TCAC) del 11,7% entre 2019 y 2027.
Los dispositivos médicos son cruciales, ya que tienen un impacto directo en la vida de los pacientes. Para brindarles una experiencia segura y de alta calidad, los fabricantes de dispositivos médicos los someten a pruebas exhaustivas antes de su comercialización. Para cumplir con las estrictas normativas, los fabricantes suelen realizar las pruebas internamente o subcontratar los servicios a organizaciones de investigación por contrato (CRO). El objetivo de las pruebas es garantizar la seguridad, la calidad y la consistencia del servicio durante todas las etapas de desarrollo y uso de los dispositivos médicos. Dado que el tratamiento médico depende en gran medida de los dispositivos médicos, es fundamental asegurar que sus pruebas se realicen con la máxima profesionalidad. El crecimiento del mercado de servicios de pruebas de dispositivos médicos en el sector sanitario se atribuye al desarrollo de productos innovadores, las colaboraciones, las fusiones y adquisiciones, y el estricto marco regulatorio para la aprobación de dispositivos médicos, factores que han impulsado el crecimiento del mercado a lo largo de los años. Asimismo, se prevé que los avances en la industria de dispositivos médicos tengan un impacto positivo en la demanda durante el período de pronóstico. Sin embargo, el crecimiento del mercado se ve limitado por factores como las interrupciones en las obligaciones contractuales.
Se espera que el mercado de servicios de pruebas de dispositivos médicos en el sector sanitario experimente un crecimiento sustancial tras la pandemia. SGS SA, Eurofins, Toxikon, Pace Analytical Services, LLC, Intertek Group plc, NORTH AMERICAN SCIENCE ASSOCIATES INC., Charles River, WuXi AppTec, Element Materials Technology, TÜV SÜD AG prevén que el ARNm emerja y transforme la industria farmacéutica, y también se espera que el mercado experimente una mayor integración vertical y empresas conjuntas en los próximos años.
Perspectivas del mercado
El creciente uso de servicios de pruebas de dispositivos médicos en el sector sanitario impulsará el crecimiento del mercado de estos servicios.
Obtendrá personalización gratuita de cualquier informe, incluyendo partes de este informe, análisis a nivel de país y paquetes de datos de Excel. Además, podrá aprovechar excelentes ofertas y descuentos para empresas emergentes y universidades.
Mercado de servicios de pruebas de dispositivos médicos: Perspectivas estratégicas

-
Obtenga las principales tendencias clave del mercado que se describen en este informe.Esta muestra GRATUITA incluirá análisis de datos, que abarcarán desde tendencias de mercado hasta estimaciones y pronósticos.
Las pruebas de dispositivos médicos requieren una amplia experiencia en el sector, conocimiento de la legislación local y nacional, e información sobre los dispositivos, la infraestructura y la capacidad para realizar las pruebas. El sector sanitario y de dispositivos médicos es muy dinámico gracias al desarrollo continuo y a las soluciones avanzadas. Los avances en la tecnología de dispositivos médicos han mejorado significativamente la eficiencia de la atención al paciente en las últimas décadas.
Sin embargo, los fabricantes de diversos dispositivos médicos a veces se enfrentan a dificultades para preparar sus productos para el mercado. Las normativas son en ocasiones complejas y difíciles de comprender, sobre todo en lo que respecta a las aplicaciones de dispositivos médicos innovadores y novedosos.
Una retirada del mercado es un proceso para eliminar o modificar productos que no cumplen con las leyes administradas por la Administración de Alimentos y Medicamentos (FDA). En la mayoría de los casos, las retiradas de dispositivos médicos son realizadas voluntariamente por la empresa, de acuerdo con el Título 21 del Código de Regulaciones Federales (CFR), Parte 7. La FDA clasifica las retiradas de productos en distintas categorías, como I, II o III, para indicar el grado de riesgo para la salud que representan.
Según la FDA, en 2018 se identificaron más de 80 000 incidentes relacionados con lesiones causadas por dispositivos médicos desde 2008. En los últimos años, las empresas de dispositivos médicos y los médicos han observado que los estimuladores de la médula espinal han ayudado a pacientes con trastornos del dolor. Por ello, se ha convertido en uno de los productos con mayor crecimiento en la industria de dispositivos médicos, valorada en 400 000 millones de dólares. En consecuencia, el aumento de las retiradas de productos y la mayor demanda de productos de calidad incrementan la necesidad de realizar pruebas a los dispositivos médicos, lo que a su vez impulsará el mercado de servicios de análisis de dispositivos médicos.
La tecnología de dispositivos médicos está mejorando la vida al identificar enfermedades en etapas tempranas y optimizar el tratamiento, el diagnóstico y el seguimiento de los pacientes. Se han implementado programas de capacitación para pequeñas y medianas empresas (pymes) en países como China, Chile, Indonesia, México, Malasia, Singapur, Filipinas, Perú, Rusia y Vietnam, entre otros. En 2018, el mercado de dispositivos médicos en el Reino Unido se valoró en aproximadamente 10.600 millones de dólares estadounidenses. De este mercado, alrededor de 2.500 son pequeñas y medianas empresas de dispositivos médicos en el Reino Unido. Además, un gran número de empresas multinacionales han establecido sus sedes centrales o filiales en el país. Asimismo, los hospitales de agudos invierten anualmente un promedio de 6.600 millones de dólares estadounidenses en suministros clínicos, que incluyen equipos médicos.
Además, en 2018, la Administración de Comercio Internacional (ITA) indicó que en Francia existen más de 1300 empresas de dispositivos médicos, de las cuales un tercio son extranjeras. Sin embargo, estas empresas extranjeras representan aproximadamente dos tercios del volumen total de negocio.
Además, de las 1300 empresas de dispositivos médicos en Francia, aproximadamente el 92 % son pequeñas y medianas empresas (pymes), de las cuales el 88 % se dedican exclusivamente a la fabricación de dispositivos médicos. Las pymes subcontratan las pruebas de sus dispositivos médicos, ya que requieren un alto coste, tiempo y mano de obra especializada.SMEs), out of which 88% produce entirely medical devices. SME’s outsource the medical device testing as it requires high cost, time, and skilled labor.
Además, Madrid y Cataluña representan más del 80 % de las ventas de dispositivos médicos. De este mercado, el 90 % corresponde a pequeñas y medianas empresas (pymes), que generan alrededor del 40 % de los ingresos totales del sector. Al ser empresas emergentes, optan por externalizar las pruebas de sus dispositivos médicos para reducir costes y ahorrar tiempo. Por lo tanto, se prevé que la creciente demanda del sector impulse el crecimiento del mercado global de servicios de pruebas de dispositivos médicos en los próximos años. Ofrecer tecnología médica avanzada a los consumidores es un objetivo prioritario.
- Esta muestra GRATUITA incluirá análisis de datos, que abarcarán desde tendencias de mercado hasta estimaciones y pronósticos.
proyecto de riesgo. Por lo tanto, las empresas ofrecen pruebas correctas al proporcionar resultados precisos y confiables para los requisitos de prueba de dispositivos médicos, desde pequeñas empresas emergentes hasta grandes fabricantes establecidos.
Muchos laboratorios de Norteamérica, Europa y Asia Pacífico ofrecen conocimientos sobre cumplimiento normativo y pruebas GMP/GLP/ISO 17025 cualificadas para garantizar tiempos de mejora rápidos utilizando el más alto nivel de servicio y las tecnologías más avanzadas para los requisitos de pruebas microbiológicas, químicas analíticas, de biocompatibilidad y de embalaje.
En otros países, existen diversos organismos reguladores que se encargan de regular los dispositivos médicos. En España, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) controla y autoriza los dispositivos médicos. La Ley de Alimentos y Medicamentos (FDA) establece un marco regulatorio para numerosos dispositivos médicos. La Oficina de Dispositivos Médicos es otro organismo responsable de las directrices que permiten la venta e importación de dispositivos médicos.
Todos los dispositivos médicos tienen un conjunto exclusivo y sistemático de requisitos de prueba impuestos por la FDA, la Administración Nacional de Productos Médicos de China (NMPA), los organismos notificados de la UE y otros organismos reguladores, que deben cumplirse antes de entrar en el mercado.
En Canadá, Health Canada implementó la notificación obligatoria de incidentes con dispositivos médicos por parte de importadores y fabricantes, e incentiva la notificación por parte de profesionales de la salud, hospitales y consumidores/pacientes. En México, la COFEPRIS es responsable de la aprobación y el registro de los dispositivos médicos. El fabricante debe cumplir con todos los requisitos de pruebas y obtener la aprobación de la COFEPRIS.
La Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) es la autoridad competente en materia de dispositivos médicos en el Reino Unido. Inspecciona los dispositivos médicos que presentan posibles problemas y garantiza su seguridad y calidad. En Japón, el Ministerio de Salud, Trabajo y Bienestar (MHLW) y la Agencia de Productos Farmacéuticos y Dispositivos Médicos (PMDA) colaboran para realizar pruebas científicas de los dispositivos médicos en proceso de comercialización y así supervisar su seguridad tras su comercialización.
Por lo tanto, se espera que las regulaciones cada vez más estrictas para dispositivos innovadores y precisos impulsen el crecimiento del mercado de servicios de pruebas de dispositivos médicos durante el período de pronóstico.
Información basada en servicios
En cuanto a los servicios, el mercado de pruebas de dispositivos médicos en el sector sanitario se segmenta en pruebas de biocompatibilidad, pruebas químicas, pruebas microbiológicas y de esterilidad, y validación de envases. En 2018, las pruebas microbiológicas y de esterilidad representaron la mayor cuota de mercado, con un 53,55 % del mercado de servicios de pruebas de dispositivos médicos.
Perspectivas regionales del mercado de servicios de pruebas de dispositivos médicos
Los analistas de The Insight Partners han explicado en detalle las tendencias regionales y los factores que influyen en el mercado de servicios de pruebas de dispositivos médicos durante el período de previsión. Esta sección también analiza los segmentos y la geografía del mercado de servicios de pruebas de dispositivos médicos en Norteamérica, Europa, Asia Pacífico, Oriente Medio y África, y Sudamérica y Centroamérica.
Alcance del informe de mercado de servicios de pruebas de dispositivos médicos
| Atributo del informe | Detalles |
|---|---|
| Tamaño del mercado en 2018 | 5.510 millones de dólares estadounidenses |
| Tamaño del mercado para 2027 | 14.660 millones de dólares estadounidenses |
| Tasa de crecimiento anual compuesto global (2018 - 2027) | 11,7% |
| Datos históricos | 2016-2017 |
| período de previsión | 2019-2027 |
| Segmentos cubiertos |
Por servicio
|
| Regiones y países cubiertos |
América del norte
|
| Líderes del mercado y perfiles de empresas clave |
|
Densidad de los participantes en el mercado de servicios de pruebas de dispositivos médicos: comprensión de su impacto en la dinámica empresarial
El mercado de servicios de pruebas de dispositivos médicos está creciendo rápidamente, impulsado por la creciente demanda de los usuarios finales debido a factores como la evolución de las preferencias de los consumidores, los avances tecnológicos y una mayor conciencia de los beneficios del producto. A medida que aumenta la demanda, las empresas amplían su oferta, innovan para satisfacer las necesidades de los consumidores y aprovechan las tendencias emergentes, lo que impulsa aún más el crecimiento del mercado.
- Obtenga una visión general de los principales actores del mercado de servicios de pruebas de dispositivos médicos.
Perspectivas basadas en fases
Según la fase, el mercado de servicios de pruebas de dispositivos médicos en el sector sanitario se divide en preclínica y clínica. En 2018, el segmento preclínico representó una cuota de mercado considerable, del 68,17%, del mercado de servicios de pruebas de dispositivos médicos, por fase.
Los actores del mercado de servicios de pruebas de dispositivos médicos en el sector sanitario están adoptando estrategias de lanzamiento y expansión de productos para satisfacer las cambiantes demandas de los clientes en todo el mundo, lo que también les permite mantener su marca a nivel global.
Servicios de prueba de dispositivos médicos en el mercado de la salud – por servicio
- Prueba de biocompatibilidad
- Prueba de química
- Microbiología y pruebas de esterilidad
- Validación de paquetes
Servicios de pruebas de dispositivos médicos en el mercado de la salud – por fase
- Preclínico
- Clínico
Servicios de prueba de dispositivos médicos en el mercado de la salud – por geografía
-
América del norte
- A NOSOTROS
- Canadá
- México
-
Europa
- Francia
- Alemania
- Italia
- Reino Unido
- España
- El resto de Europa
-
Asia Pacífico (APAC)
- Porcelana
- India
- Corea del Sur
- Japón
- Australia
- Resto de Asia Pacífico
-
Oriente Medio y África (MEA)
- Sudáfrica
- Arabia Saudita
- Emiratos Árabes Unidos
- Resto de Oriente Medio y África
-
Sudamérica y Centroamérica (ESTAFA)
- Brasil
- Argentina
- El resto es ESTAFA
Perfiles de empresas
- SGS SA
- Eurofins
- Toxicon
- Servicios Analíticos Pace, LLC
- Grupo Intertek plc
- ASOCIADOS CIENTÍFICOS DE NORTEAMERICANO INC.
- Río Charles
- Tecnología de aplicaciones WuXi
- Tecnología de materiales elementales
- TÜV SÜD AG
- Análisis histórico (2 años), año base, pronóstico (7 años) con CAGR
- Análisis PEST y FODA
- Tamaño del mercado, valor/volumen: global, regional y nacional
- Industria y panorama competitivo
- Conjunto de datos de Excel
Testimonios
Razón para comprar
- Toma de decisiones informada
- Comprensión de la dinámica del mercado
- Análisis competitivo
- Información sobre clientes
- Pronósticos del mercado
- Mitigación de riesgos
- Planificación estratégica
- Justificación de la inversión
- Identificación de mercados emergentes
- Mejora de las estrategias de marketing
- Impulso de la eficiencia operativa
- Alineación con las tendencias regulatorias





















 Obtenga una muestra gratuita para - Mercado de servicios de pruebas de dispositivos médicos
Obtenga una muestra gratuita para - Mercado de servicios de pruebas de dispositivos médicos