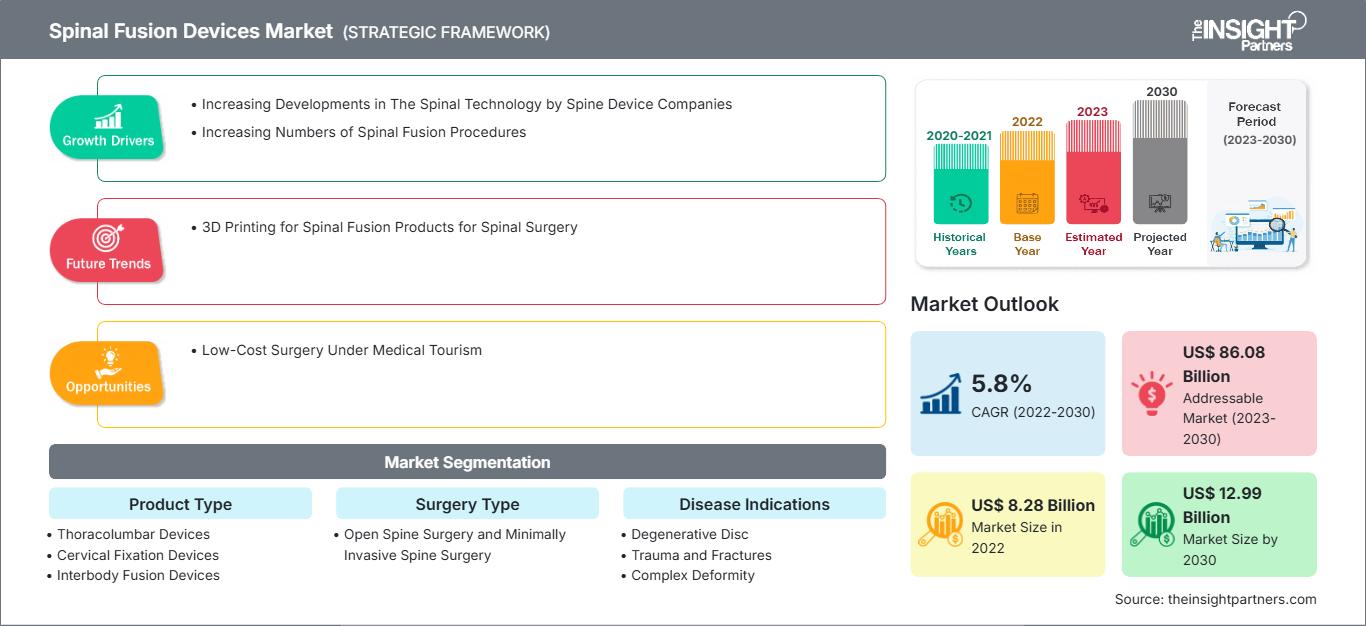
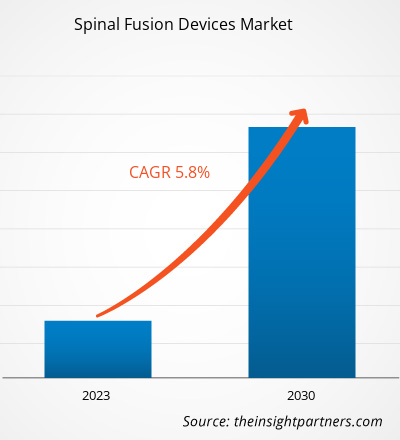
[연구 보고서] 척추 유합 장치 시장 규모는 2022년 82억 7,631만 달러에서 2030년 129억 9,325만 달러로 성장할 것으로 예상되며, 2022년부터 2030년까지 연평균 5.8% 성장할 것으로 예상됩니다.
시장 분석 및 분석가 의견:
담석 발생 증가로 인한 척추 유합 장치 시술 건수 증가로 척추 유합 장치 시장 규모가 빠르게 성장하고 있습니다. 또한 당뇨병 발생률 증가 또한 시장 성장을 촉진하고 있습니다.
또한, 시장 개발을 위한 기업들의 전략적 이니셔티브 또한 시장 성장을 촉진하고 있습니다. 2022년 9월, GE 헬스케어는 3D 및 PROPELLER 영상 시퀀스를 위한 혁신적인 AIR Recon DL에 대한 미국 FDA 510(k) 승인을 발표했습니다. AIR Recon DL의 장점은 이러한 새로운 기능을 통해 거의 모든 자기공명영상(MRI) 임상 시술로 확장되어 모든 해부학적 구조를 포괄하고 더 나은 영상 품질, 더 짧은 스캔 시간, 그리고 향상된 환자 경험을 제공합니다. 따라서 고객 요구를 충족하는 혁신적인 기술의 급격한 증가는 예측 기간 동안 시장에 새로운 트렌드를 가져올 것으로 예상됩니다.
기회와 과제:
척추 유합술은 비용이 훨씬 더 많이 들기 때문에 많은 환자가 척추 수술 결정을 미루고 있습니다. 또한, 많은 경우 척추 임플란트 비용이 건강 보험에 포함되지 않아 수술 횟수가 제한적입니다. 예를 들어 미국과 같은 나라는 물가가 높습니다. 2022년 2월에 발표된 Healthcare Bluebook 데이터에 따르면, 요추 척추 유합술 비용이 가장 높은 상위 5개 도시는 다음과 같습니다. 덴버: 미화 86,182달러, 캘리포니아주 산호세: 미화 78,809달러, 샌프란시스코: 미화 78,809달러, 인디애나폴리스: 미화 77,269달러, 시애틀: 미화 74,499달러. 동시에, 요추 척추 유합술의 최소 비용은 테네시주 멤피스와 샌안토니오와 같은 도시에서 약 미화 48,000달러입니다.
이 보고서의 일부, 국가 수준 분석, Excel 데이터 팩을 포함하여 모든 보고서에 대한 사용자 정의를 무료로 받을 수 있을 뿐만 아니라 스타트업 및 대학을 위한 훌륭한 제안 및 할인을 이용할 수 있습니다
척추 융합 장치 시장: 전략적 통찰력
-
이 보고서의 주요 주요 시장 동향을 확인하세요.이 무료 샘플에는 시장 동향부터 추정 및 예측에 이르기까지 데이터 분석이 포함됩니다.
한편, 의료 관광은 척추 유합술을 더 저렴한 비용으로 제공할 수 있게 해 주었습니다. 개발도상국 국가들은 의료 관광을 크게 발전시켰고, 세계적인 수준의 의료 서비스를 더 저렴한 가격으로 제공하는 첨단 기술을 보유하고 있습니다. Lyfboat Technologies Pvt.가 2023년 7월에 발표한 자료에 따르면 인도, 태국, 터키, UAE, 이집트와 같은 국가들은 미화 8,000달러에서 16,000달러 사이의 척추측만증 수술을 제공하는 데 가장 적합한 것으로 나타났습니다. Lyfboat Technologies Pvt.가 발표한 자료에 따르면 이집트의 척추 유합술 비용은 미화 10,897달러, UAE의 경우 약 미화 8,200달러입니다. 마찬가지로 터키의 척추 유합술 비용은 미화 15,000달러, 인도의 경우 약 미화 8,000달러에서 12,000달러 사이입니다. 또한 인도의 흉곽성형술 비용은 미화 2,500달러에서 4,000달러 사이입니다.
중요한 수술을 저렴한 비용으로 제공함으로써 이러한 국가로의 환자 유입이 증가하고 있습니다. 또한, 첨단 의료 기술의 보급과 의료 관광 확대를 위한 정부 지원금 증가로 첨단 수술용 임플란트 수요가 증가하고 있습니다. 더 나아가, 개발도상국의 의료 인프라 발전은 첨단 의료기기에 대한 수요를 지속시켜 척추 유합 장치 시장의 성장 기회를 확대할 것으로 예상됩니다.
척추 유합 장치에 대한 규제 요건은 다른 이식형 장치와 다릅니다. 척추 유합 장치 규정은 환자의 삶의 질을 향상시키기 위해 제품의 품질을 유지하기 위해 정기적으로 업데이트됩니다. 2023년 3월, 미국 식품의약국(FDA)은 의료기기, 정형외과 기기, 추간 유합술용 척추구 분류(최종 규칙)의 최종 규제 영향 분석을 업데이트했습니다. FDA 분석에 따르면 척추 기기는 3등급으로 분류됩니다. 이 기기들은 시판 전 승인 신청을 위해 별도의 서류 제출이 필요합니다. 또한, FDA는 일반 및 특별 관리만으로는 기기의 효과와 안전성을 보장하기에 불충분하다고 판단했습니다. 따라서 기업들은 제품의 재질, 크기 및 임상적 상태의 의도에 대한 사양과 관련된 혼란을 피하기 위해 제품 효율성 및 안전성에 대한 완전한 제품 설명과 분석을 제공해야 할 것으로 예상됩니다.
마찬가지로, 개발도상국의 규정 또한 척추 유합술 기기에 대한 규제 요건을 업데이트하고 있습니다. 2021년 11월, 호주 보건복지부 산하 노인치료의약품관리국(TGA)은 척추 이식형 의료기기에 대한 규제 체계를 개정했습니다. TGA는 새로운 규제 요건을 갖춘 스폰서와 제조업체가 업데이트된 요건을 이해하고 준수할 수 있도록 지원하는 것을 목표로 합니다. TGA는 제조업체에 네 가지 주요 요건을 제시했는데, 여기에는 ARTG 항목에 2b등급 척추 유합술 기기에 대한 구체적인 정보 제공 의무, 임상적 증거 평가를 포함한 기기 포함 신청에 대한 TGA의 의무 감사 평가 등이 포함됩니다. 기기 분류에 대한 적절한 절차를 입증하는 적합성 평가 문서와 각 기기와 관련된 품질 관리 시스템 및 기술 문서에 대한 제조업체의 철저한 평가가 필요합니다. 따라서 제조업체에 대한 엄격한 규정은 더 많은 경제적 투자로 이어질 것이며, 리콜 위험은 손실로 이어질 수 있습니다. 따라서 척추 유합 장치에 대한 엄격한 규정은 시장 성장을 저해하는 요인 중 하나입니다.
보고서 세분화 및 범위:
척추 유합 장치 시장 점유율은 제품 유형, 수술 유형, 질병 적응증 및 최종 사용자를 기준으로 구분됩니다. 척추 유합 장치 시장은 제품 유형별로 흉요추 장치, 경추 고정 장치, 추체간 유합 장치로 세분화됩니다. 수술 유형별로 척추 유합 장치 시장은 개방형 척추 수술과 최소 침습 척추 수술로 구분됩니다. 질병 적응증별로 척추 유합 장치 시장은 퇴행성 디스크, 외상 및 골절, 복합 기형 등으로 세분화됩니다. 척추 유합술 기기 시장은 최종 사용자별로 병원, 전문 클리닉 등으로 세분화됩니다. 지리적으로 볼 때, 시장은 북미(미국, 캐나다, 멕시코), 유럽(영국, 독일, 프랑스, 이탈리아, 스페인 및 기타 유럽), 아시아 태평양(중국, 일본, 인도, 한국, 호주 및 기타 아시아 태평양), 중동 및 아프리카(UAE, 사우디아라비아, 남아프리카 및 기타 중동 및 아프리카), 중남미(브라질, 아르헨티나 및 기타 중남미)로 구분됩니다.
세분화 분석:
척추 유합술 기기 시장은 수술 유형에 따라 개복 척추 수술과 최소 침습 척추 수술로 나뉩니다. 2022년에는 개복 척추 수술 부문이 수술 부문에서 더 큰 시장 점유율을 차지했습니다. 최소 침습 척추 수술 분야는 최소 침습 척추 수술 접근법의 도입 증가로 인해 2022년부터 2030년까지 더 높은 연평균 성장률(CAGR)로 성장할 것으로 예상됩니다. 개방 수술은 해부학적 구조에 완전히 노출될 수 있기 때문에 표준 수술로 간주됩니다. 개방 척추 수술은 척추 측만증, 디스크의 심각한 퇴행, 척추 불안정성 또는 이러한 문제의 조합과 같은 질환을 치료하는 데 권장됩니다. 질환이 심각하고 복잡한 경우 개방 수술이 널리 선호됩니다. 해부학적 구조에 더 많이 노출되어 시술이 용이하고 주변 구조를 더 잘 볼 수 있습니다. 그러나 개방 척추 수술에는 여러 가지 위험이 있습니다. 위험에는 과도한 출혈과 긴 회복 시간이 포함됩니다.
많은 경우 개방 척추 수술 유형은 척추 질환의 증상을 역전시킬 수 있습니다. 합병증으로 인해 감염, 상처 치유 불량, 혈전, 주변 정맥 또는 신경 손상이 발생할 수도 있습니다.
최소 침습 척추 수술 유형(MISS)은 기존의 개방 척추 수술 유형보다 주목할 만한 관심을 받고 있습니다. MISS는 더 작은 절개를 필요로 합니다. 따라서 MISS 시술을 받도록 환자를 설득하는 것이 더 쉬워졌습니다. 주변 근육 손상 방지, 출혈 감소, 통증 감소, 빠른 회복, 입원 기간 단축 등의 다른 장점들도 MISS 도입을 증가시켰습니다. 현재 MISS는 척추 유합술의 일반적인 시술로 여겨지고 있습니다. MISS 도입률 증가에는 위험을 최소화하고 보험금 지급 방식과 환자 선호도를 변화시킴으로써 고령자 및 중증 환자의 척추 문제를 치료하는 것이 포함됩니다. 또한, MISS의 혁신은 강력한 소프트웨어를 결합한 새로운 수술 중 영상 기술을 도입했습니다. 영상 기술과 소프트웨어의 결합은 외과의가 척추의 3차원(3D) 해부학적 구조에 대한 이해를 보완할 수 있도록 실시간 탐색 기능을 제공합니다. 따라서 MISS의 혁신은 해당 분야의 가장 빠른 성장으로 이어지고 있으며, 궁극적으로 시장 성장을 촉진하고 있습니다. 2022년 7월에 발표된 "최소 침습 척추 수술 유형: 개요"라는 제목의 기사에 따르면, 미국에서 매년 120만 건의 척추 시술 중 약 75%가 MISS 기술을 통해 시행됩니다. 마찬가지로, 2022년 1월에 발표된 "척추 내시경: 증거, 기술, 세계 동향 및 미래 전망"이라는 논문에서는 아시아 외과의의 96.7%가 최소침습수술(MISS)을 시행한다고 밝혔습니다. 따라서 MISS 시술 건수가 증가하는 것을 고려할 때, 향후 몇 년 동안 시장이 눈에 띄게 성장할 것으로 예상됩니다. 척추 유합 장치 시장은 제품 유형별로 흉요추 장치, 경추 고정 장치, 추체간 유합 장치로 구분됩니다. 2022년에는 흉요추 장치 부문이 제품 유형별로 시장 점유율이 가장 높았습니다. 추체간 유합 장치 부문은 추체간 유합 장치 개발 증가로 인해 2022년부터 2030년까지 상당한 연평균 성장률(CAGR)을 기록할 것으로 예상됩니다. 척추 유합 장치 시장은 질병 적응증별로 퇴행성 디스크, 외상 및 골절, 복합 기형 등으로 분류됩니다. 2022년, 퇴행성 디스크 부문은 질병 지표 기준으로 시장에서 가장 큰 점유율을 차지했으며, 퇴행성 질환에 걸리기 쉬운 고령 인구 증가로 인해 2022년부터 2030년까지 상당한 연평균 성장률(CAGR)로 성장할 것으로 예상됩니다. 척추 유합술 시장은 최종 사용자 기준으로 병원, 전문 클리닉, 기타로 구분됩니다. 2022년에는 병원 부문이 시장에서 가장 큰 점유율을 차지했으며, 향후 몇 년 동안 가장 빠른 속도로 성장할 것으로 예상됩니다.
지역 분석:
지리적 분포를 기준으로 척추 유합술 시장은 북미, 유럽, 아시아 태평양, 중동 및 아프리카, 중남미로 구분됩니다. 북미는 시장 성장에 가장 큰 기여를 하고 있으며, 아시아 태평양은 가장 빠르게 성장하는 지역입니다. 북미의 척추 유합술 시장은 미국, 캐나다, 멕시코로 구분됩니다. 2022년에 미국은 이 지역에서 가장 큰 시장 점유율을 기록했으며 예측 기간 동안에도 지배력을 유지할 것으로 예상됩니다. DePuy Synthes, Stryker, Aurora Spine, Alevio Spine은 미국 척추 융합 장치 시장에서 활동하는 주요 기업입니다. 이러한 기업이 주도하는 제품 개발 및 출시는 시장 성장을 촉진합니다. 미국 식품의약국(FDA)에서 승인한 기술적으로 진보된 척추 융합 장치는 미국에서 널리 채택되고 있습니다. 다음은 최근 FDA에서 승인한 척추 융합 장치 목록입니다.
- 2023년 5월, CTL Amedica는 생체재료인 질화규소를 융합하여 독점적으로 만든 NITRO Interbody Fusion Cage System의 상용화를 위한 FDA 510(k) 승인을 받았습니다. 질화규소 소재는 모든 영상 모달리티와 호환됩니다. 이 제품은 독특한 정균 특성을 나타내며 인공물 없는 영상을 제공합니다.
- 2023년 1월, Alevio Spine은 SI-Cure SI 관절 유합 시스템에 대한 추가 적응증에 대해 510(K) 허가를 받았습니다. 이 확대된 적응증에는 요추 또는 흉요추 유합술의 일환으로 천골반 고정술을 받는 골격 성숙 환자를 위한 천장골 유합술이 포함됩니다.
- 2022년 6월, 미국 FDA는 Aurora Spine의 DEXA SOLO-L 전방 요추 추체간 유합 장치(ALIF)에 대해 510K 허가를 부여했습니다. DEXA 기술 플랫폼을 기반으로 3D 프린팅된 독립형 장치가 전방 및 외측 요추 추체간 유합술(ALIF & LLIF)을 위해 설계되었습니다.
연령에 따른 마모는 미국 노인 인구의 요통(LBP) 유병률을 증가시키고, 이는 척추 유합술 장비 수요를 증가시킵니다. 2022년 미국 국민건강보험공단(NHS)에 따르면, 미국에서 평생 요통 발생률은 60~90%로 보고되었으며, 연간 발생률은 5%입니다. 또한, 매년 신규 환자의 14.3%가 요통으로 인해 병원을 방문하고, 약 1,300만 명이 만성 요통으로 병원을 방문한다고 합니다.
척추 융합 장치 시장 지역별 통찰력
The Insight Partners의 분석가들은 예측 기간 동안 척추 유합 장치 시장에 영향을 미치는 지역별 동향과 요인들을 면밀히 분석했습니다. 이 섹션에서는 북미, 유럽, 아시아 태평양, 중동 및 아프리카, 그리고 중남미 지역의 척추 유합 장치 시장 부문 및 지역별 현황도 다룹니다.
척추 유합 장치 시장 보고서 범위
| 보고서 속성 | 세부 |
|---|---|
| 시장 규모 2022 | US$ 8.28 Billion |
| 시장규모별 2030 | US$ 12.99 Billion |
| 글로벌 CAGR (2022 - 2030) | 5.8% |
| 이전 데이터 | 2020-2021 |
| 예측 기간 | 2023-2030 |
| 다루는 세그먼트 |
By 제품 유형
|
| 포함된 지역 및 국가 |
북미
|
| 시장 선도 기업 및 주요 회사 프로필 |
|
척추 융합 장치 시장 참여자 밀도: 비즈니스 역학에 미치는 영향 이해
척추 유합 장치 시장은 소비자 선호도 변화, 기술 발전, 그리고 제품 효능에 대한 인식 제고 등의 요인으로 인한 최종 사용자 수요 증가에 힘입어 빠르게 성장하고 있습니다. 수요가 증가함에 따라 기업들은 제품 라인업을 확장하고, 소비자 니즈를 충족하기 위한 혁신을 추진하며, 새로운 트렌드를 적극 활용하고 있으며, 이는 시장 성장을 더욱 가속화하고 있습니다.
- 을 얻으세요 척추 융합 장치 시장 주요 주요 플레이어 개요
척추 유합 장치 시장에서 활동하는 주요 업체들의 다양한 사업 계획은 다음과 같습니다.
- 2023년 2월, 저명한 근골격계 솔루션 제공업체인 Globus Medical Inc와 척추 기술 혁신의 선구자인 NUVASIVE는 주식 합병을 통해 합병하기로 합의했습니다. 이 거래를 통해 환자 치료 개선을 위한 미충족 임상 요건을 끊임없이 추구하는 혁신이라는 공통된 비전을 가진 두 유명 근골격계 기술 회사가 하나로 모이게 되었습니다.
- 2022년 11월, Centinel Spine LLC는 prodisc C SK 경추 추간판 치환술(TDR) 제품의 첫 이식을 발표했습니다. prodisc C SK 시스템은 출시될 세 가지 신제품 중 두 번째 제품입니다.
- 2022년 3월, DePuy Synthes Inc는 CUPTIMIZE Hip-Spine Analysis를 인수하여 외과의에게 인공 고관절 전치환술(THA)이 필요한 일부 환자에서 척추와 골반 사이의 비정상적인 가동성이 미치는 영향을 더 잘 이해하고 해결할 수 있는 사용하기 쉬운 도구를 제공했습니다. CUPTIMIZE Hip-Spine Analysis는 DePuy Synthes의 VELYS Digital Surgery 연결 기술 플랫폼 중 하나인 VELYS Hip Navigation의 수술 계획 기능을 향상시킵니다.
경쟁 환경 및 주요 기업:
척추 유합 장치 시장에서 활동하는 몇몇 주요 기업으로는 Medtronic PLC, Johnson & Johnson, Inc., 그리고 Johnson Services Inc, B.Braun SE, Stryker Corp, ATEC Spine Inc, Globus Medical Inc, NuVasive Inc, ZimVie Inc, Centinel Spine LLC, Orthofix Medical Inc. 이 회사들은 전 세계적으로 증가하는 소비자 수요를 충족하고 전문 포트폴리오의 제품 범위를 확대하기 위해 신제품 출시 및 지역 확장에 집중하고 있습니다. 글로벌 네트워크를 통해 다양한 고객에게 서비스를 제공하고, 궁극적으로 시장 점유율을 확대하고 있습니다.
- 과거 분석(2년), 기준 연도, CAGR을 포함한 예측(7년)
- PEST 및 SWOT 분석
- 시장 규모 가치/거래량 - 글로벌, 지역, 국가
- 산업 및 경쟁 환경
- Excel 데이터세트
최근 보고서
사용 후기
구매 이유
- 정보에 기반한 의사 결정
- 시장 역학 이해
- 경쟁 분석
- 고객 인사이트
- 시장 예측
- 위험 완화
- 전략 기획
- 투자 타당성 분석
- 신흥 시장 파악
- 마케팅 전략 강화
- 운영 효율성 향상
- 규제 동향에 발맞춰 대응





















 무료 샘플 받기 - 척추 융합 장치 시장
무료 샘플 받기 - 척추 융합 장치 시장