Der Markt für Monozyten-Aktivierungstests wird bis 2031 voraussichtlich ein Volumen von 1.630 Millionen US-Dollar erreichen. Es wird erwartet, dass der Markt im Zeitraum 2025–2031 eine durchschnittliche jährliche Wachstumsrate (CAGR) von 14,6 % verzeichnen wird.
Analystensicht
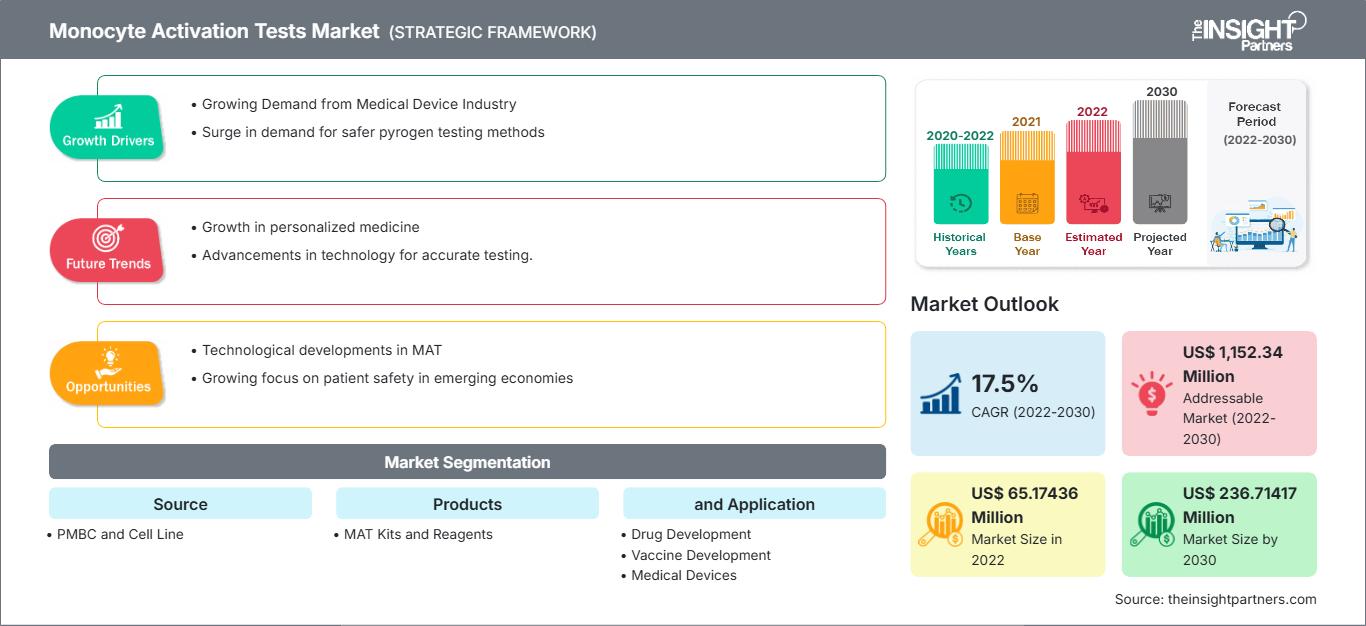
Die Marktanalyse für Monozytenaktivierungstests umfasst die Untersuchung von Markttreibern wie dem gestiegenen Sicherheitsbewusstsein der Patienten und der zunehmenden Nachfrage nach sichereren Pyrogen-Testmethoden in Endverbraucherbranchen wie der Pharma-, Biotechnologie- und Medizintechnikbranche. Darüber hinaus wird erwartet, dass technologische Entwicklungen bei Monozytenaktivierungstestmethoden das Marktwachstum im Prognosezeitraum weiter ankurbeln werden.
Basierend auf der Quelle ist der Markt für Monozytenaktivierungstests in PMBC und Zelllinien unterteilt. Das PMBC-Segment hatte 2022 den größeren Marktanteil und wird diesen Trend voraussichtlich im Prognosezeitraum fortsetzen. Basierend auf den Produkten ist der Markt für Monozytenaktivierungstests in MAT-Kits und Reagenzien unterteilt. Das Segment der MAT-Kits hatte 2022 den größeren Marktanteil und wird diesen Trend voraussichtlich im Prognosezeitraum fortsetzen. Demgegenüber wird für das Reagenziensegment im Prognosezeitraum eine höhere durchschnittliche jährliche Wachstumsrate (CAGR) erwartet. Basierend auf der Anwendung ist der Markt für Monozytenaktivierungstests in Arzneimittelentwicklung, Impfstoffentwicklung, Medizinprodukte und Sonstiges (Forschung etc.) unterteilt. Das Segment der Arzneimittelentwicklung hatte 2022 den größten Marktanteil und wird diesen Trend voraussichtlich von 2022 bis 2030 beibehalten.
Der Monozytenaktivierungstest (MAT) detektiert eine verstärkte Zytokinfreisetzung, die durch den synergistischen Effekt von Endotoxin und Nicht-Endotoxin-Pyrogenen hervorgerufen wird. Der MAT ist ein In-vitro-Assay zur Prüfung parenteraler Arzneimittel, Biologika und Medizinprodukte auf Pyrogene aller Klassen. In den letzten fünf Jahren zählten Impfstoffe, die zuvor den Kaninchen-Pyrogentest als Freisetzungsassay verwendeten, zu den ersten Anwendern des MAT. Im Gegensatz zum MAT sind bakterielle Endotoxintests häufig ungeeignet für Produkte, die von Natur aus pyrogen sind oder Zusatzstoffe wie Aluminiumhydroxid enthalten, die häufig in Impfstoffen vorkommen und den Test stören können. Beispiele für die Anwendung des MAT bei Impfstoffen sind Impfstoffe gegen Neisseria meningitidis, Hyperimmunserum, Meningokokken-Impfstoffe, Gelbfieberimpfstoff, Shigella sonnei-Impfstoff, Tollwutimpfstoff, Hepatitis-B-Impfstoff und Impfstoff gegen Frühsommer-Meningoenzephalitis (FSME).
Passen Sie diesen Bericht Ihren Anforderungen an.
Kostenlose AnpassungMarkt für Monozyten-Aktivierungstests: Strategische Einblicke
-
Ermitteln Sie die wichtigsten Markttrends dieses Berichts.Diese KOSTENLOSE Probe beinhaltet eine Datenanalyse, die von Markttrends bis hin zu Schätzungen und Prognosen reicht.
Markteinblicke
Wachsende Nachfrage aus der Medizintechnikbranche
Monozytenaktivierungstests (MATs) sind zellbasierte Tests mit menschlichen Zellen zum Nachweis und zur Quantifizierung von Pyrogenen wie Bakterien, Pilzen und Viren. MATs nutzen einen ELISA-Test zur Messung der Zytokinfreisetzung aus behandelten Blutzellen. MATs sind weit verbreitet, werden aber selten anstelle von Tierversuchen zur Beurteilung der Biokompatibilität von Medizinprodukten eingesetzt. Das National Toxicology Program Interagency Center for the Evaluation of Alternative Toxicological Methods (NICEATM) und das PETA International Science Consortium Ltd. (PISC) veranstalteten im September 2018 einen Workshop an den National Institutes of Health, um die notwendigen Schritte zur Implementierung von MATs in der Prüfung von Medizinprodukten zu erörtern. Laut Luxoft, einem Unternehmen von DXC Technology, tragen Medizinprodukte zur digitalen Transformation des Gesundheitswesens bei, indem sie durch prädiktive Algorithmen und Patientendatenanalyse präzise Diagnosen, effektive Behandlungen und personalisierte Versorgung ermöglichen. Technologische Fortschritte in der personalisierten Medizin, bei implantierbaren Geräten, intelligenten Medizinprodukten und minimalinvasiver Chirurgie revolutionieren das gesamte Gesundheitswesen durch bessere Versorgung, verbesserte Patientenergebnisse und geringere Kosten. Das Wachstum der Medizintechnikbranche hat wiederum das Wachstum von Testmethoden zur Monozytenaktivierung in der Gegenwart ermöglicht und dürfte diesen Trend im Prognosezeitraum fortsetzen.
Marktchance
Technologische Entwicklungen bei Testmethoden zur Monozytenaktivierung
Die Monozytenaktivierungstestmethode (MAT) wurde hauptsächlich als Alternative zu Tierversuchen eingeführt, um Pyrogentests in einem humanen In-vitro-System zu ermöglichen. Nach der Veröffentlichung internationaler Validierungen wurde der MAT 2010 in das Europäische Arzneibuch (EP) aufgenommen. Kontinuierliche Innovationen und Weiterentwicklungen der MAT-Assays und -Reagenzien durch Marktteilnehmer haben die Reproduzierbarkeit, Sensitivität und Spezifität wesentlich verbessert und ihn somit zu einer zuverlässigen und sichereren Option für den Pyrogennachweis gemacht. Der MAT-Assay dient dem Nachweis von Endotoxinen und Nicht-Endotoxin-Pyrogenen in parenteralen Produkten wie Arzneimitteln und Medizinprodukten. Üblicherweise stellt der MAT eine In-vitro-Alternative zu traditionellen Tierversuchen im Einklang mit den regulatorischen Richtlinien dar. Der Kaninchenpyrogentest und der Limulus-Amöbozytenlysat-Test (LAL-Test) werden häufig zum Pyrogennachweis eingesetzt. Beide Methoden verwenden Tiere und weisen einige Einschränkungen auf. Der Kaninchenpyrogentest ist weniger robust, da die Reaktion des Tieres von der des Menschen abweichen kann. Darüber hinaus werden im LAL-Test nur Endotoxine nachgewiesen, wodurch andere Pyrogene, die möglicherweise in der Probe vorhanden sind, unberücksichtigt bleiben und somit ein Sicherheitsrisiko darstellen. Um diese Einschränkungen zu überwinden, wurde der Monozyten-Aktivierungstest (MAT) 2010 in die Europäische Pharmakopöe als Arzneibuchmethode aufgenommen und ersetzte den Kaninchen-Pyrogentest (EP Kapitel 2.6.30). Auch die FDA empfiehlt ihn in ihren Leitlinien für die Industrie. Kontinuierliche Innovationen und Weiterentwicklungen der MAT-Tests und -Reagenzien durch Marktteilnehmer haben die Reproduzierbarkeit, Sensitivität und Spezifität deutlich verbessert und ihn somit zu einer zuverlässigen und sichereren Option für den Pyrogennachweis gemacht.
Berichtssegmentierung und -umfang
Quellenbasierte Erkenntnisse
Basierend auf der Quelle ist der Markt für Monozytenaktivierungstests in PMBC und Zelllinien unterteilt. Das PMBC-Segment hatte 2022 den größeren Marktanteil und wird diesen Trend voraussichtlich im Prognosezeitraum fortsetzen. Für dieses Segment wird von 2022 bis 2030 ein höheres durchschnittliches jährliches Wachstum (CAGR) erwartet. Weltweit sind derzeit zwei kommerzielle Zellquellen für Monozytenaktivierungstests verfügbar: die Mono-Mac-6 (MM6)-Zelllinie und periphere mononukleäre Blutzellen (PBMC). Die MM6-Zelllinie stammt aus dem Blut eines einzelnen Patienten mit akuter monozytärer Leukämie. Daher weisen die Monozyten mitunter keine TLRs auf, deren stabile Expression für den zuverlässigen Nachweis pyrogener Kontaminanten und die Auslösung der Zytokinfreisetzung durch einen gesunden Menschen erforderlich ist. Aus diesem Grund ist die Reproduzierbarkeit von MAT-Ergebnissen mit dieser Zellquelle gering. Das Europäische Arzneimittel-Institut (Ph. Eur., 2.6.30) beschreibt MM6-basierte MAT-Kits ebenfalls als „eingeschränkt“ in ihrer Fähigkeit, nicht-endotoxinartige Pyrogene nachzuweisen. Andererseits beziehen PBMC-basierte MAT-Kits ihre PBMC aus dem gepoolten Blut von untersuchten, gesunden Spendern. Das bedeutet, dass die Monozytenaktivierung bei Inkubation mit einer angereicherten Produktprobe das Wachstum eines gesunden Menschen fördern kann. Daher sind die Ergebnisse von MAT-Kits, die auf dieser Zellquelle basieren, durchweg reproduzierbar. Das Europäische Arzneibuch (Ph. Eur., 2.6.30) stuft diese Zellquelle als geeignet für den Nachweis von Endotoxinen und nicht-endotoxinischen Pyrogenen ein.
Derzeit sind drei weitere Anbieter kommerzieller PBMC-basierter Monozytenaktivierungstests auf dem Markt. Die Nachweisgrenzen (LoD) liegen bei 0,125 EU/ml, 0,02 EU/ml bzw. 0,016 EU/ml. Der CTL-MAT-Assay weist mit 0,004 EU/ml eine der marktführenden Nachweisgrenzen auf und ist damit der weltweit sensitivste verfügbare Monozytenaktivierungstest.
Produktbasierte Erkenntnisse
Basierend auf den Produkten ist der Markt für Monozytenaktivierungstests in MAT-Kits und Reagenzien unterteilt. Das Segment der MAT-Kits hatte 2022 den größeren Marktanteil und wird diesen Trend voraussichtlich im Prognosezeitraum fortsetzen. Das Segment der Reagenzien hingegen dürfte im Prognosezeitraum eine höhere durchschnittliche jährliche Wachstumsrate (CAGR) verzeichnen.
Anwendungsbasierte Erkenntnisse
Basierend auf der Anwendung ist der Markt für Monozytenaktivierungstests in Arzneimittelentwicklung, Impfstoffentwicklung, Medizinprodukte und Sonstiges (Forschung etc.) unterteilt. Das Segment Arzneimittelentwicklung hatte 2022 den größten Marktanteil und wird diesen Trend voraussichtlich von 2022 bis 2030 fortsetzen. Laut der National Library of Medicine sind Arzneimittel eine Gruppe neuartiger organischer Verbindungen, die zur Verbesserung der Lebensqualität von Patienten beigetragen haben. Der Pharmasektor ist in der Produktion, Entwicklung und Vermarktung von Marken- und Generika-Arzneimitteln tätig. 2014 überstiegen die weltweiten Pharmaumsätze erstmals 1 Billion US-Dollar. Der Pharmamarkt wächst seit 2017 jährlich um 5,8 %. Im selben Jahr betrug der weltweite Umsatz des Pharmamarktes 1.143 Milliarden US-Dollar und erreichte 2021 1.462 Milliarden US-Dollar. Der Monozytenaktivierungstest (MAT) dient der Prüfung von parenteralen Arzneimitteln, Biologika und Medizinprodukten auf alle Pyrogenklassen. Parenteral verabreichte Arzneimittel müssen frei von pyrogenen (fieberauslösenden) Verunreinigungen sein, da diese Substanzen eine lebensbedrohliche systemische Reaktion des angeborenen Immunsystems des Patienten hervorrufen können. Es ist sicherzustellen, dass biologische Produkte vor der Verabreichung an Patienten frei von pyrogenen Verunreinigungen sind. Anfänglich wurden der RPT (Reverse Provocacy Test) und der bakterielle Endotoxintest (BET)/Limulus-Amöbozytenlysat-Test (LAL) als Ex-vivo-Optionen eingesetzt. Strenge Vorschriften für Tierversuchsmethoden haben die Marktteilnehmer jedoch gezwungen, eine alternative Methode zu entwickeln, die den Einsatz solcher Tierversuche minimiert. Angesichts der Einschränkungen des RPT und des BET sowie der zunehmenden Herstellung komplexer Produkte führte die Europäische Pharmakopöe MAT-Aktivierungstestmethoden ein, die die humane Immunantwort simulieren und die Vorteile des RPT (Beurteilung der Pyrogenität über gramnegative Endotoxine hinaus) mit den Vorteilen einer In-vitro-Methode kombinieren. Im Gegensatz zum RPT kann der MAT als vollständig quantitativer Test ohne Tierversuche durchgeführt werden. Dadurch eignet er sich besonders für Impfstoffe, die von Natur aus pyrogen sind und aufgrund der Verwendung menschlicher Zellen physiologisch relevant sind. Mit MAT-Testverfahren lassen sich Blutprodukte, Zellprodukte, Biologika und Impfstoffe nachweisen. Die MAT-Testmethoden eignen sich auch für eine breite Palette von Arzneimitteln und Medizinprodukten sowie für Produkte, die nicht in vivo getestet werden können (z. B. Produkte mit Hyaluronsäure). Diese Faktoren haben den Markt für Monozytenaktivierungstests in den letzten Jahren positiv beeinflusst und werden voraussichtlich auch im Prognosezeitraum einen ähnlichen Trend fortsetzen.
Markteinblicke in Monozyten-Aktivierungstests
Die regionalen Trends und Einflussfaktoren auf den Markt für Monozyten-Aktivierungstests im gesamten Prognosezeitraum wurden von den Analysten von The Insight Partners eingehend erläutert. Dieser Abschnitt behandelt außerdem die Marktsegmente und die geografische Verteilung des Marktes für Monozyten-Aktivierungstests in Nordamerika, Europa, Asien-Pazifik, dem Nahen Osten und Afrika sowie Süd- und Mittelamerika.
Umfang des Marktberichts zu Monozyten-Aktivierungstests
| Berichtattribute | Details |
|---|---|
| Marktgröße im Jahr 2024 | XX Millionen US-Dollar |
| Marktgröße bis 2031 | 1.629,80 Millionen US-Dollar |
| Globale durchschnittliche jährliche Wachstumsrate (2025 - 2031) | 14,6 % |
| Historische Daten | 2021-2023 |
| Prognosezeitraum | 2025–2031 |
| Abgedeckte Segmente |
Nach Quelle
|
| Abgedeckte Regionen und Länder |
Nordamerika
|
| Marktführer und wichtige Unternehmensprofile |
|
Marktteilnehmerdichte bei Monozyten-Aktivierungstests: Auswirkungen auf die Geschäftsdynamik verstehen
Der Markt für Monozyten-Aktivierungstests wächst rasant, angetrieben durch die steigende Nachfrage der Endverbraucher. Gründe hierfür sind unter anderem sich wandelnde Verbraucherpräferenzen, technologische Fortschritte und ein wachsendes Bewusstsein für die Vorteile des Produkts. Mit steigender Nachfrage erweitern Unternehmen ihr Angebot, entwickeln innovative Lösungen, um den Kundenbedürfnissen gerecht zu werden, und nutzen neue Trends, was das Marktwachstum zusätzlich beflügelt.
- Verschaffen Sie sich einen Überblick über die wichtigsten Akteure auf dem Markt für Monozyten-Aktivierungstests.
Regionalanalyse
Basierend auf den Regionen ist der Markt für Monozytenaktivierungstests in Nordamerika, Europa, Asien-Pazifik, Süd- und Mittelamerika sowie den Nahen Osten und Afrika unterteilt. Nordamerika hielt 2022 den größten Marktanteil und wird diesen Trend voraussichtlich im Prognosezeitraum fortsetzen, gefolgt von Europa. Regulatorische Maßnahmen von Organisationen wie der United States Pharmacopeia (USP) und der kanadischen Regierung haben das Wachstum des Marktes für Monozytenaktivierungstests in der Region zusätzlich beflügelt. Auch der zunehmende Fokus auf Patientensicherheit und verbesserte Behandlungsergebnisse trägt zum Marktwachstum in Nordamerika bei.
Zu den führenden Unternehmen auf dem Markt für Monozytenaktivierungstests zählen Merck KGaA, Darmstadt, Deutschland und/oder ihre Tochtergesellschaften; Charles River Laboratories International, Inc.; Thermo Fisher Scientific; Sanquin; und die Lonza-Gruppe.
Im Oktober 2023 brachte Lonza zwei neue Schnelltests zur Monozytenaktivierung (MAT) auf den Markt: das PyroCell MAT Rapid System und das PyroCell MAT Human Serum (HS) Rapid System. Diese Systeme vereinfachen und beschleunigen die Pyrogenprüfung ohne Tierversuche. Sie ersetzen die bisherigen MAT-Testkits von Lonza und enthalten den neuen PeliKine Human IL-6 Rapid ELISA Kit. Dieser minimiert den Arbeitsaufwand und verkürzt die Zeit bis zum Ergebnis von zwei Tagen auf zwei Stunden. Pharma- und Biotechnologieunternehmen profitieren von den neuen Tests, die die MAT-Testung ihrer Produkte vereinfachen und gleichzeitig die Abhängigkeit von Tierversuchen reduzieren.
- Historische Analyse (2 Jahre), Basisjahr, Prognose (7 Jahre) mit CAGR
- PEST- und SWOT-Analyse
- Marktgröße Wert/Volumen – Global, Regional, Land
- Branchen- und Wettbewerbslandschaft
- Excel-Datensatz
Erfahrungsberichte
Grund zum Kauf
- Fundierte Entscheidungsfindung
- Marktdynamik verstehen
- Wettbewerbsanalyse
- Kundeneinblicke
- Marktprognosen
- Risikominimierung
- Strategische Planung
- Investitionsbegründung
- Identifizierung neuer Märkte
- Verbesserung von Marketingstrategien
- Steigerung der Betriebseffizienz
- Anpassung an regulatorische Trends














Exklusive Berichtsrabatte freischalten
Jetzt anfragen






 Kostenlose Probe anfordern für - Markt für Monozytenaktivierungstests
Kostenlose Probe anfordern für - Markt für Monozytenaktivierungstests